Amazonが書類提出を求める背景を理解しておく重要性
Amazon.comで健康食品やサプリメントなどを販売していると、ある日突然「Document Request」という通知が届くことがある。商品の出品が止まり、指定された書類を提出しなければ再開できない――この状況に直面して、慌てて対処しようとするセラーは少なくない。
しかし、ここで焦って「とにかく何か出す」と動いてしまうと、追加質問が重なり、対応が長期化しやすい。重要なのは、Amazonがなぜ書類を求めているのか、その「意図」を正しく理解し、目的に合った資料を揃えることにある。
本記事では、Amazonの書類提出要求にまつわる典型的な誤解を整理したうえで、提出書類を「目的別」に捉える考え方、実務上の注意点、そして事前に備えておくべき対策について解説する。
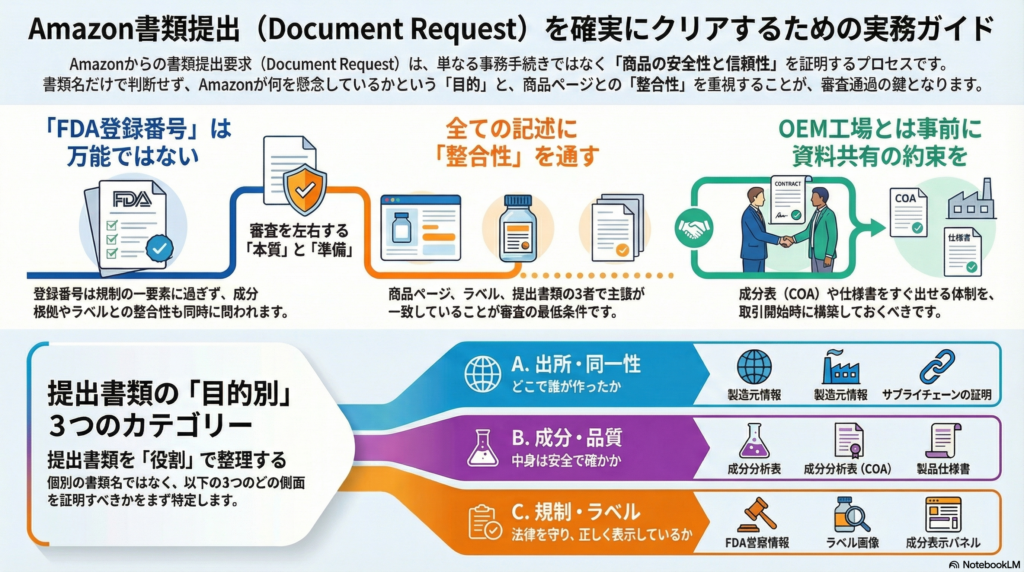
「FDA登録番号さえあれば通る」は本当か?よくある6つの誤解
Document Requestに関しては、ネット上にさまざまな情報が飛び交っており、それが誤解の温床になっている。まずは、多くのセラーが陥りやすい典型的な思い込みを確認しておきたい。
FDA登録番号だけで足りるという思い込み
「FDA登録番号を提出すれば解除される」という情報を見かけることがある。しかし、登録番号はあくまで規制面の一要素に過ぎず、Amazonが確認したい内容が成分の根拠やラベル表示の整合性であれば、登録番号だけでは要求に応えたことにならない可能性がある。
どの商品でも同じ書類で通るという思い込み
提出書類は商品カテゴリや商品ページ上の主張(クレーム)によって変わり得る。あるサプリメントで通った書類セットが、別のカテゴリの商品にそのまま使えるとは限らない。「テンプレを出せば通る」という発想は、追加質問を招く原因になりやすい。
形式さえ整えれば内容は問われないという思い込み
書類のフォーマットが整っていても、商品ページの記載内容と提出資料の間に矛盾があれば、審査は通りにくい。見た目の体裁よりも、「商品ページで言っていること」と「書類で示していること」の一貫性が問われやすい。
代行業者に任せれば把握しなくてよいという思い込み
代行業者を活用すること自体は問題ないが、「何をどういう根拠で提出したか」を自分で説明できない状態は危うい。追加質問が来た際に対応方針が立てられず、長期化の原因になりやすい。
書類を出せば必ず解除されるという思い込み
提出はゴールではなくスタート地点に近い。内容に不足や矛盾があれば追加の問い合わせが発生し得る。「出せば終わり」ではなく、「出した書類に対して何を聞かれても説明できる状態」を目指す方が現実的である。
Amazonの要求と行政の要求を混同する思い込み
AmazonのDocument Requestは、プラットフォーム独自の購入者保護・リスク管理の観点から発せられるものであり、FDAや通関(CBP)の行政照会とは目的が異なる場合がある。同じ「書類提出」でも、求めている主体と確認したい内容が違い得るという点を意識しておきたい。
Amazonが書類提出を求める目的とは|購入者保護とリスク管理の視点
Amazonがセラーに書類を求める根底にある考え方を押さえておくと、個別の要求にも対処しやすくなる。
一般的に、Amazonが書類提出を求めるのは「購入者保護」と「リスク管理」の観点から、その商品が安全に流通し得るか、商品ページの主張に根拠があるかを確認したい場合と考えられる。つまり、Amazonは「この書類が欲しい」以上に、「この商品は大丈夫か」を確認したいのであり、書類はその確認手段に過ぎない。
この視点を持つだけで、「どの書類を出すか」ではなく「何を証明すればいいのか」に思考が切り替わり、対処精度が上がりやすい。
提出書類を「目的別」に整理する4つのカテゴリ
提出を求められる書類を個別の書類名で丸暗記しようとすると、状況が変わったときに応用が効かない。ここでは、実務上有用な「目的別の4分類」で整理する。
(A)製品の同一性・出所の確認
「その商品はどこの誰が作ったものか」を示すための書類群である。製造元の情報、サプライチェーン上の取引関係、商品の同一性を証明する資料などがここに含まれ得る。OEM商品の場合、工場との関係を示す書類が求められることもある。
(B)成分・仕様・品質の根拠
「中身は何で、品質の裏付けはあるか」を示すための書類群である。成分表(Certificate of Analysis)、製品仕様書、品質試験の結果などが該当し得る。特に健康食品やサプリメントでは、成分の安全性や含有量の根拠が重視される傾向がある。
(C)規制・コンプライアンス関連
「必要な規制上の登録や届出をしているか」「責任主体は明確か」を示す書類群である。FDA施設登録やUS Agent情報、NDI(新規ダイエタリー成分)通知などがカテゴリによっては関連し得る。ただし前述のとおり、登録情報だけで全ての要求が満たされるわけではない。
(D)ラベル・表示の確認
「消費者に対してどのような情報を表示しているか」を示す書類群である。実際のラベル画像、Supplement Facts Panel、注意書きの記載内容などが含まれ得る。商品ページの記載とラベルの記載が一致しているかどうかも確認対象になりやすい。
この4分類を頭に入れておくと、Document Requestが届いた際に「今回の要求はA~Dのどこに該当するのか」を切り分けやすくなり、的外れな書類を提出するリスクを減らせる可能性がある。
実務で問題になりやすい6つの落とし穴
書類提出の段階で実際につまずきやすいポイントを整理する。事前に認識しておくだけで、対応の質が変わり得る。
要求の意図を取り違えて的外れな書類を出す
Amazonが品質の根拠を求めているのに登録情報だけを出す、規制面の確認なのに成分表だけを出す、といった「要求と回答のズレ」は追加質問の典型的な原因になる。まず「何を確認したいのか」を読み解くことが出発点である。
商品ページの主張と提出資料の不一致
商品ページで謳っている効能や用途が、提出した書類の内容と噛み合わない場合、書類自体が正当であっても解除されにくい。たとえば、ページ上で特定の健康効果を示唆しているのに、提出資料にその裏付けがなければ整合性が問われやすい。
OEM商品で必要資料がすぐに揃わない
OEM・輸入販売の場合、成分情報、製造仕様、品質試験結果などの情報が製造工場側にあり、セラーの手元にない場合がある。いざDocument Requestが来てから工場に資料を依頼すると、時差やコミュニケーションコストも加わり、対応が長引きやすい。
登録情報を出して安心してしまう
FDA施設登録やNDI通知があること自体は重要だが、それが「免罪符」になるわけではない。登録があっても、商品ページの表現やラベル表示との整合性が弱ければ、追加の確認が入り得る。登録はあくまで規制面の一要素として位置づけるのが妥当である。
焦って商品ページを大幅に改変してしまう
書類提出と並行して、慌てて商品ページの表現を大きく変えてしまうケースがある。提出資料は変更前の商品ページの記載を前提にしている場合、ページを書き換えたことで新たな矛盾が生まれ、かえって状況が複雑化しやすい。変更するなら、提出資料との整合性を確認してからが望ましい。
代行業者に任せきりで説明できない状態になる
外部業者に委託すること自体は合理的な判断だが、「何をどの根拠で提出したのか」を自分で把握していないと、追加質問への対応が遅れやすい。少なくとも提出書類のリストと、各書類が何を証明するためのものかは、自分でも整理しておくことが望ましい。
事前準備で長期化を防ぐ|5つの予防策
Document Requestは突然届くが、事前の備えによって対応のスピードと精度は大きく変わり得る。
書類を「書類名」ではなく「目的」で整理しておく
「COAを用意する」「FDA登録番号を控える」といった書類名ベースの準備だけでなく、前述の4分類(出所・成分品質・規制・ラベル)のどれに対応する資料かを整理しておくと、要求が来たときに迷いにくい。
商品の用途を1文で固定し、一貫性を保つ
「この商品は何であり、何のために使うものか」を1文で明確に定義し、商品ページ・ラベル・提出資料のすべてでその定義からブレないようにする。主張の筋が通っているほど、審査側からの追加質問が減る傾向がある。
OEMの場合は工場から出せる資料を事前に確認する
いざ要求が来てから工場に連絡するのでは遅い場合がある。取引開始時点で、COA・製造仕様書・品質試験結果などの提出可否と、発行までのリードタイムを確認しておくと、有事の際に対応が早まりやすい。
AmazonのDocument Requestと通関照会を分けて考える
Amazonからの書類要求と、通関時のCBP・FDA照会は、似たような書類を求められることがあるが、目的と提出先が異なる。混同すると「どの書類がどこ向けか」が分からなくなりやすいため、提出先ごとに整理しておくのが安全である。
変更管理を前提にした運用体制を持つ
SKU追加、商品ページの表現変更、ラベルリニューアルなどが発生するたびに、既存の提出資料との整合性が崩れるリスクがある。「一度通ったら終わり」ではなく、変更が入るたびに資料の整合性をチェックする仕組みを持っておくと、再発防止につながりやすい。
まとめ|書類提出は「目的の理解」と「整合性の維持」がカギ
AmazonのDocument Requestに対応する際に最も重要なのは、個別の書類名を暗記することではなく、「Amazonが何を確認したいのか」という要求の意図を正しく読み解くことである。
提出書類は商品カテゴリや商品ページの主張によって変わり得るため、万能なテンプレートは存在しにくい。だからこそ、書類を目的別(出所・成分品質・規制・ラベル)に整理し、商品ページの記載内容との一貫性を保つことが、審査をスムーズに進めるための基本になる。
また、FDA登録などの規制対応は重要な要素だが、それだけで全てが解決するわけではない。表現やラベルとの整合性が伴ってこそ、登録情報が活きてくる。
OEM商品を扱うセラーは特に、工場側が保有する資料の範囲と提出可否を事前に確認しておくことで、有事の際の初動を早められる可能性がある。