はじめに
米国食品医薬品局(FDA)における化粧品規制は、2022年の化粧品規制近代化法(MoCRA)成立により大きな転換期を迎えている。全施設登録の義務化や重篤な有害事象報告の15日以内提出など、企業に求められるコンプライアンス要件は飛躍的に増大した。こうした規制強化の流れと並行して、FDAは業務全般にAI技術を積極的に導入し始めており、化粧品分野の検査・品質管理においてもその影響は無視できないものとなっている。
本記事では、FDAにおけるAI活用の現状、AI導入がもたらす検査体制と審査プロセスの変化、規制当局のスタンスとガイダンスの動向を整理する。さらに、日本の化粧品メーカーがこの潮流をどう捉え、どのような機会と課題に直面するのか、そして今後3〜5年で予想される技術進化とトレンドについて展望する。
米国FDAにおけるAI活用の現状
全部門へのAI展開計画
FDAは2025年に全ての部門でAIを内部展開する計画を打ち出した。新薬審査での試行では、従来3日を要していた作業を数分で完了する成果が示されており、その有効性は明らかである。この全社的なAI推進には化粧品分野も含まれ、職員向けに生成AIツール(大規模言語モデル)や「Agentic AI」プラットフォームが提供されている。品質・安全担当者や査察官がデータ分析や手続きにAIを利用できる環境整備が進められており、特に査察(Inspection)やコンプライアンス業務へのAI適用が重視されている。
MoCRAによる規制強化とデジタル対応
化粧品は医薬品ほど事前承認制度が厳格ではなかったが、MoCRAにより監督権限は大幅に強化された。全ての化粧品施設登録・製品リスト提出、安全性実証データの備蓄、重篤な有害事象の15日以内報告が義務化され、FDAによるリコール命令権限も明文化されている。こうした規制強化とデジタル報告の増大に対応するため、FDAはAIを活用して提出データのチェックや市場監視を効率化する取り組みを加速している。
化粧品ガイダンス文書へのAI適用
FDA内部では化粧品に関するガイダンス文書の検索効率向上を目的としたGenerative AIの実証実験が行われている。2025年には化粧品ガイダンス文書へのアクセス改善を競うAIアプリコンテストも開催された。さらに、2020年のFDA共催コロキウムでは工場洗浄プロセスへのAI技術や機械学習による化粧品成分の安全性評価が議論されており、FDA自身がAI技術を業務に組み込みつつ、化粧品企業側にも高度なデジタル対応を求める方向性が明確になっている。
AI導入によって変わる検査体制と審査プロセス
製造現場における検査の自動化・高度化
人手による目視検査は属人的で見逃しやバラツキの問題があったが、ディープラーニングを用いた画像解析により微細な傷や異物の検出精度が飛躍的に向上している。ある調査では、AI画像認識を検査に使うことで生産性が最大50%向上し、欠陥検出率は人間の目視比で最大90%も改善したと報告されている。
化粧品はパッケージや中身に複雑な模様・質感を持つ製品が多く、従来のルールベース検査では正常パターンと欠陥の区別が困難であった。AI活用により、複雑な模様や凹凸のある化粧品表面に混入した微細な異物もパターンのばらつきを学習することで見逃さず検出できるようになった。人では識別しにくいランダム模様中の傷や髪の毛もAIなら判別可能で、ラメ入りや多数の色を持つ製品でも異物を検出し、立体的な製品も360度全方位から検査できると報告されている。
プロセス全体のデータ解析によるリスク評価
画像認識AIによる外観検査では異物混入・キズ・印字ミスなど様々な外観上の不良を自動判定でき、ヒト検査では困難だった微小粒子の検出や品質ばらつきの定量評価も可能になっている。さらに、製造プロセス全体のデータをAI解析することでリスク評価の高度化が図られている。センサーデータや検査記録を機械学習モデルにかけて異常傾向を早期に検知し、設備の予防保全やロットの出荷停止判断に役立てる試みである。
製造オペレーションの各種データストリームとAIを連携すれば、初期段階で品質リスクを指摘したり、発生しうる問題を自動検知できるため、従来は事後対応だったトラブルへの事前予防的な検査体制が構築できる。
審査プロセスにおけるAI補助
医薬品分野では既に申請資料のAI解析やレビューワークの自動化が進み、新薬審査の時間短縮に寄与している。化粧品分野でも、成分や配合データをAIで解析してリスク評価を行い、当局や社内の承認判断をサポートすることが考えられる。
市場で収集される消費者クレームや有害事象報告のテキストマイニングにもAIが有効である。大量のクレーム・SNS投稿・レビューを自然言語処理AIでリアルタイム分析することで、従来は埋もれていた製品トラブルの兆候を早期にシグナル検出できる。例えば皮膚トラブルに関する投稿増加や特定ロットに集中する苦情をAIが察知すれば、企業はリコールや改善対応を迅速に講じられ、FDAへの報告義務にもスムーズに対処できる可能性がある。
AIに関する規制とFDAのスタンス
慎重な支持と厳格な管理要求
FDAのスタンスは一貫して「革新的技術の活用を歓迎するが、規制上の基本原則は緩めない」というものである。FDAはAI自体を禁止する考えはなく、品質予測、検査自動化、根本原因解析などへのAI活用を慎重に支持しているが、その前提としてデータの信頼性確保やモデルのバリデーション、説明可能性などを強く求めている。AIが関与する判断は他の検証済みプロセスと同様の厳格さで管理されねばならないとし、出力に対する人間の監視や記録の完全性(監査証跡)を重視している。
ガイダンスとリスクベースフレームワーク
現時点でAIそのものを直接規制する詳細ルールは整備途上だが、FDAは関連業界に向けたガイダンスを通じて徐々に枠組みを示している。2025年1月には「医薬品・生物製剤の規制判断を支援するAI活用」に関するガイダンス草案が発出され、安全性・有効性・品質評価に用いるAIモデルの信頼性を確保するためのリスクベースフレームワークが提示された。このガイダンスでは文脈に応じたモデルの「信頼性評価」を推奨しており、AIを用いたデータ提出時にはモデルの適格性を証明することが求められる。
医療機器分野でも、FDAはAI搭載ソフトの変更管理計画(PCCP)に関する指針を示すなど、製品ライフサイクルにおけるAIの管理方法を整備中である。
既存規制の枠内での評価
製造現場や検査工程で使われるAIアルゴリズムについては、現状明確な個別規制は無く既存のGMPや品質システム規制の枠内で評価されている。EUではGMP付属書でAIについて言及する動きもあるが、FDAも含め各国当局は「AI搭載の検査機も従来機器同様、既知の欠陥を既定精度で検出できるようバリデーションせよ」との基本姿勢を崩していない。要するに「AIだから特別扱いはしないが、ちゃんと性能を証明すれば活用を認める」というアプローチである。
最新のAI検査装置では検査結果の詳細ログやモデルの判断根拠を記録する機能を備え、監査に耐えるよう設計されている。こうした機能によりAIがブラックボックスではなく、適切に管理された品質保証プロセスの一部として位置付けられることが重要である。
実証事例と計算毒性学的アプローチ
FDA公式の実証事例としては、上述の内部レビュー業務へのAI適用(AIアシスト審査)や、PrecisionFDAを通じた外部コンテストなどがある。化粧品分野固有の事例はまだ限られるが、民間では大手化粧品企業がAIによる動物代替試験や毒性予測モデルを開発し、安全性実証に活用する動きもある。EUでの動物実験禁止も相まって、AI駆動の構造活性相関(QSAR)モデルで成分の皮膚浸透性や刺激性を予測し、安全性評価に役立てる研究も進んでいる。FDAもこうした計算毒性学的アプローチに注目しており、将来的には企業から提出されるAI解析データを審査に組み込む可能性がある。
日本の化粧品メーカーにとってのAI活用機会と課題
機会(メリット)
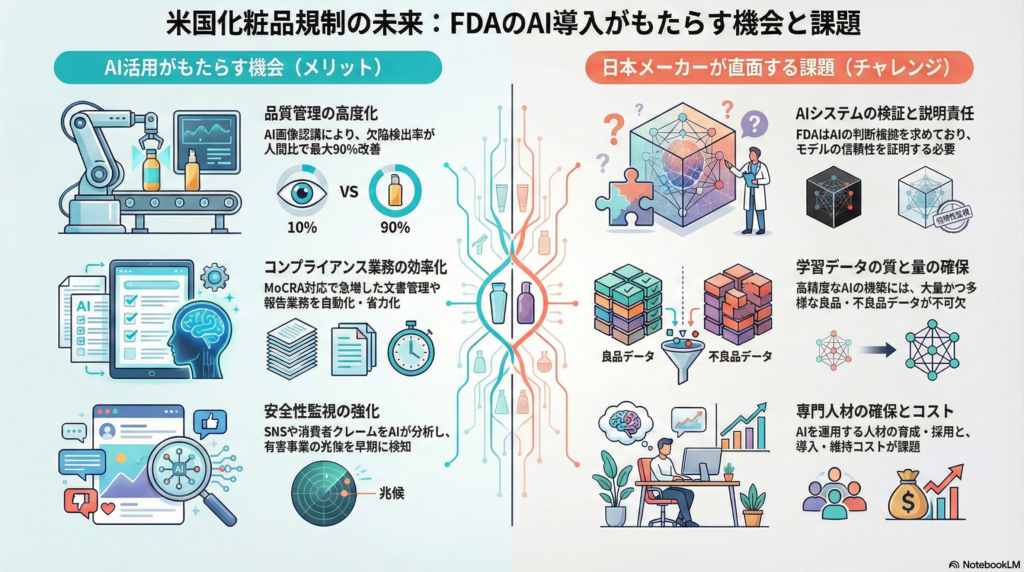
品質管理の高度化: AIによる自動外観検査やインラインモニタリング導入により製品不良の早期発見と是正が可能となり、FDA査察時の指摘リスク低減に繋がる。検査精度・効率が飛躍することでリコールや輸入差止めを未然防止し、安定供給とブランド信頼性維持に寄与する。
コンプライアンス業務の効率化: MoCRA対応で必要となる膨大な文書管理や報告業務にAI搭載の電子品質管理システム(eQMS)を用いることで、人手によるエラーや漏れを削減できる。ある調査では約26%の規制担当者が依然スプレッドシート等の手作業に頼っているとされ、急増する規制要件に追いつけない現状がある。AI駆動ツールを使えば、最新の規制情報の自動モニタリングやラベル・成分規制の即時チェックが可能となり、製品上市までの時間短縮や手戻り防止によるコスト削減が期待できる。
安全性監視(コスメトビジランス)の強化: AIを活用した自動安全性モニタリング基盤は、グローバルに散在する有害事象情報や消費者フィードバックをリアルタイム分析し、潜在的リスクのシグナルを早期に検知する。消費者苦情、皮膚科症例報告、SNS投稿などを集約しアルゴリズムで解析することで、重大な健康被害に発展する前に原因ロットの出荷停止や自主回収を判断できる。結果としてFDAへの重大有害事象報告の迅速化と的確な対応が可能となり、当局との信頼関係構築にもつながる。
安全性実証データの充実: AIモデルを活用すれば、新成分や処方の安全性を動物実験に頼らず予測評価することも可能になる。これは欧米で求められる安全性実証書類の整備に有益であり、MoCRA下で必須となった「充分な安全性裏付け」を効率よく蓄積できる。さらに将来的にFDAが計算毒性データを評価に組み込むようになれば、こうした事前のAI評価が革新的製品の迅速な上市を後押しする可能性がある。
競争優位と市場信頼: 規制対応にAIをいち早く取り入れた企業は、変化への適応力や説明責任の遂行能力で競合に優位に立てる。実際、既に39%の企業がAIを規制対応に利用し、近い将来68%が利用拡大を計画しているとの調査結果もある。いち早くAIを導入した企業は発売遅延の回避や法規制違反リスクの低減によって得たリソースを商品イノベーションに振り向けられ、結果的に市場での差別化につながると指摘されている。
課題(チャレンジ)
AIシステムのバリデーションと説明責任: AIを品質管理やデータ分析に組み込む際、そのモデルが常に正確かつ信頼できることを証明しなければならない。FDAはデータインテグリティやモデルの検証可能性を重視しており、企業側はモデルのバリデーション手順書の整備や定期的な再評価・ドリフト監視といった体制を構築する必要がある。また、ブラックボックスなAIでは当局や取引先の理解を得られないため、判断根拠を人間が解釈できる形で提示(Explainable AI)する工夫も欠かせない。
学習データの質と量の確保: ディープラーニングモデルの性能は学習データに大きく依存する。不良検出や予測モデル構築には、良品・不良品の大量かつ多様な画像やデータセットを用意する必要がある。最先端の異物検出AIでは数百万枚規模の画像で訓練を行うケースも報告されており、中小企業には自社データだけでこれを揃えるのは困難である。十分なデータを収集・生成するには、データ拡張技術の活用や業界内でのデータ共有の仕組みなどが求められる。またデータのアノテーション精度もモデル精度に直結するため、専門知識を持った人材によるデータ精査が必要である。
人材と組織体制の整備: AI導入にはデータサイエンスやITに明るい人材が不可欠だが、製造現場や品質保証部門にはそのような人材が不足しがちである。既存スタッフへの教育訓練に加え、新たにデジタル人材の採用や育成を図る必要がある。また組織文化の面でも、現場担当者がAIの提案を活用し意思決定できるよう権限移譲やワークフローの見直しが求められる。企業内でもAIツールへの信頼醸成が課題であり、導入にあたっては段階的なトレーニングとKPI設定(例:精度向上率や工数削減効果の測定)によって社内の合意形成を図ることが重要とされている。
規制動向の不確実性: AIに関する規制や基準は今後も発展途中であり、現在は問題なく使えている手法が将来の法整備で追加要求を課される可能性もある。EUではAI規制法案やGMP付属書でのAI要件策定が進行中であり、グローバルに事業展開する場合は各地域の動向をウォッチしてシステム適合性をアップデートしていく必要がある。またサイバーセキュリティや個人情報の扱いについても規制強化が見込まれ、AIシステムへのサイバーリスク対策やデータ匿名化など横断的なコンプライアンス対応が課題となる可能性がある。
コストとROIの確保: 最先端のAIソリューション導入には初期投資や運用コストが伴う。中小規模のメーカーにとって、自社専用にシステム構築するのは負担が大きいため、クラウド型サービスの活用やパートナー企業との協業によるコスト分散を検討する必要がある。また投資に見合ったリターンを得るには、導入前に明確なKPI設定と費用対効果分析を行い、段階的導入で効果を検証しつつスケールさせていく戦略が求められる。
今後3〜5年のトレンドと技術進化の見通し
規制と標準化の動向
FDAを含む各国規制当局は、AIに関するガイドライン整備とグローバル調和を進めていく見込みである。ISOやICHといった国際的枠組みでも議論が進み、地域差の少ない包括的なAIガバナンスが模索されるだろう。特に、モデルの透明性(Explainability)の確保やライフサイクル管理の義務化がキーワードとなり、企業にはAIモデルの継続的モニタリングと定期レポート、そして判断根拠の説明責任が求められる方向である。
またサイバーセキュリティやデータガバナンスへの要求も高まり、AIが扱うデータの出所管理やプライバシー保護について明確な基準が定められる可能性がある。今後は「精度が高いだけでは不十分で、理解可能で安全・公正なAIか」という観点での監督が強まると考えられる。こうした規制環境に適合するには、企業は現在のうちから説明可能性や公平性に配慮したAI開発・運用プロセスを整えておく必要がある。
技術革新と導入拡大
技術面では、ディープラーニングのさらなる高性能化とエッジAIの発展が見込まれる。ハードウェアの進歩やアルゴリズム改良により、リアルタイム画像処理でより微小な欠陥を検出したり、動画ストリーム解析で立体物内部の異常を発見するなど、現在は難しい検査も可能になっていく可能性がある。既にAI検査では複数アングルから取得した画像を動画として解析し、動きや視点差分から良否判断を下す高度手法が登場している。今後3〜5年でこうした技術が汎用化すれば、化粧品の充填過程での異物検知や外装パッケージの全数スキャンなども自動化が進むだろう。
またマルチモーダルAIの進展により、画像だけでなく匂い・音・振動センサーデータなど複合情報から異常検知・品質予測を行うシステムも登場すると考えられる。例えば、製造ラインの音響パターンと製品検査画像を組み合わせて分析し、機械の異常振動が微小な容器欠陥につながる兆候をリアルタイムに察知するといった応用が現実味を帯びている。
業界への浸透
AI導入率は今後さらに上昇し、業界標準のツールとなっていく可能性が高い。大多数の企業がAI活用を拡大予定とされており、特にグローバルに事業を展開する大手各社は独自のAIプラットフォームを構築し始めている。日本企業も含め、2025年前後から始まったMoCRA対応の経験を経て、デジタルトランスフォーメーション戦略の一環としてAIを位置付ける企業が増えると見られる。
製造現場では協働ロボットとAI検査の組み合わせによるフルオートメーションラインが試験導入され、検査員の役割はシステム監督やデータ解析へと変わっていくだろう。また、市場対応ではAIチャットボットによる消費者からの問い合わせ分析やSNSトレンド予測などマーケティング・CS領域でもAI活用が進み、収集した市場データを品質改善にフィードバックする循環が生まれる可能性がある。さらに、生成AIの発展により規制文書の自動作成や翻訳、研究報告の要約などバックオフィス業務の効率化も一層進むだろう。
FDAも内部の手続にAIを組み込み、2025年以降はより迅速な対応が期待される。こうした中で、対応が遅れた企業はコンプライアンス面での遅延が競争力低下に直結するため、各社が競って最新技術を取り入れる流れが加速すると予想される。
持続可能性と倫理の潮流
AIとESG(環境・社会・ガバナンス)の連携もトレンドとなる可能性がある。サプライチェーン最適化やエネルギー効率向上にAIを使い環境負荷低減を図る動きや、AIによる成分代替提案でグリーンケミストリーを推進する試みが増えると考えられる。またAIの判断に偏りや差別がないか監査するAI倫理委員会の設置など、企業の社会的責任の観点からの取り組みも求められるだろう。
例えば、肌色や人種によってAIの検出精度に差が出ないよう学習データの多様性を確保するといった配慮である。これらは一見規制対応とは離れた話題に見えるが、「安全で公平なAI」を実現することが長期的なブランド価値につながるとの認識が広まっており、FDAを含む規制当局も企業の倫理的AI活用を注視し始めている。
まとめ
米国FDAにおける化粧品分野へのAI導入は、規制強化と技術革新が交差する重要な転換点にある。MoCRAによる監督権限の強化とデジタル報告の増大を背景に、FDAは業務全般にAIを組み込み、検査・審査プロセスの効率化と高度化を推進している。画像解析による自動外観検査、製造プロセス全体のデータ解析によるリスク評価、消費者クレームのテキストマイニングなど、AI技術は品質管理と安全性監視の中核を担う存在となりつつある。
日本の化粧品メーカーにとって、AI活用は品質管理の高度化、コンプライアンス業務の効率化、安全性監視の強化、競争優位の確保という大きな機会をもたらす。一方で、AIシステムのバリデーションと説明責任、学習データの質と量の確保、人材と組織体制の整備、規制動向の不確実性、コストとROIの確保といった課題も存在する。
今後3〜5年では、規制と標準化の国際的調和、ディープラーニングやエッジAIのさらなる高性能化、マルチモーダルAIの登場、業界全体へのAI浸透、そして持続可能性と倫理への配慮が主要なトレンドとなるだろう。AI技術は化粧品業界の品質・安全管理の中核を担う存在となり、その恩恵を最大化するには規制順守と技術革新の両輪をバランス良く推進することが重要である。
企業は現在のうちから説明可能性や公平性に配慮したAI開発・運用プロセスを整え、段階的な導入とKPI設定による効果検証を通じて、変化する規制環境に適応していく必要がある。
コメント