はじめに:表示を信じるだけでは守れない化粧品の安全性
化粧品の成分表示は消費者にとって最も重要な安全情報です。しかし米国食品医薬品局(FDA)が公表するリコール事例を見ると、ラベルに記載されていない成分が混入していたケースが後を絶ちません。特にOEM製造された化粧品では、製造工程での成分取り違えや意図的な無許可添加により、深刻な健康被害をもたらす事例が複数報告されています。
本記事では、FDAが実際に対応した代表的なリコール事例を取り上げ、どのような未申告成分が混入し、どんな健康リスクがあったのかを詳しく解説します。さらに越境ECや個人輸入を利用する際の具体的な注意点についても実例をもとに紹介します。
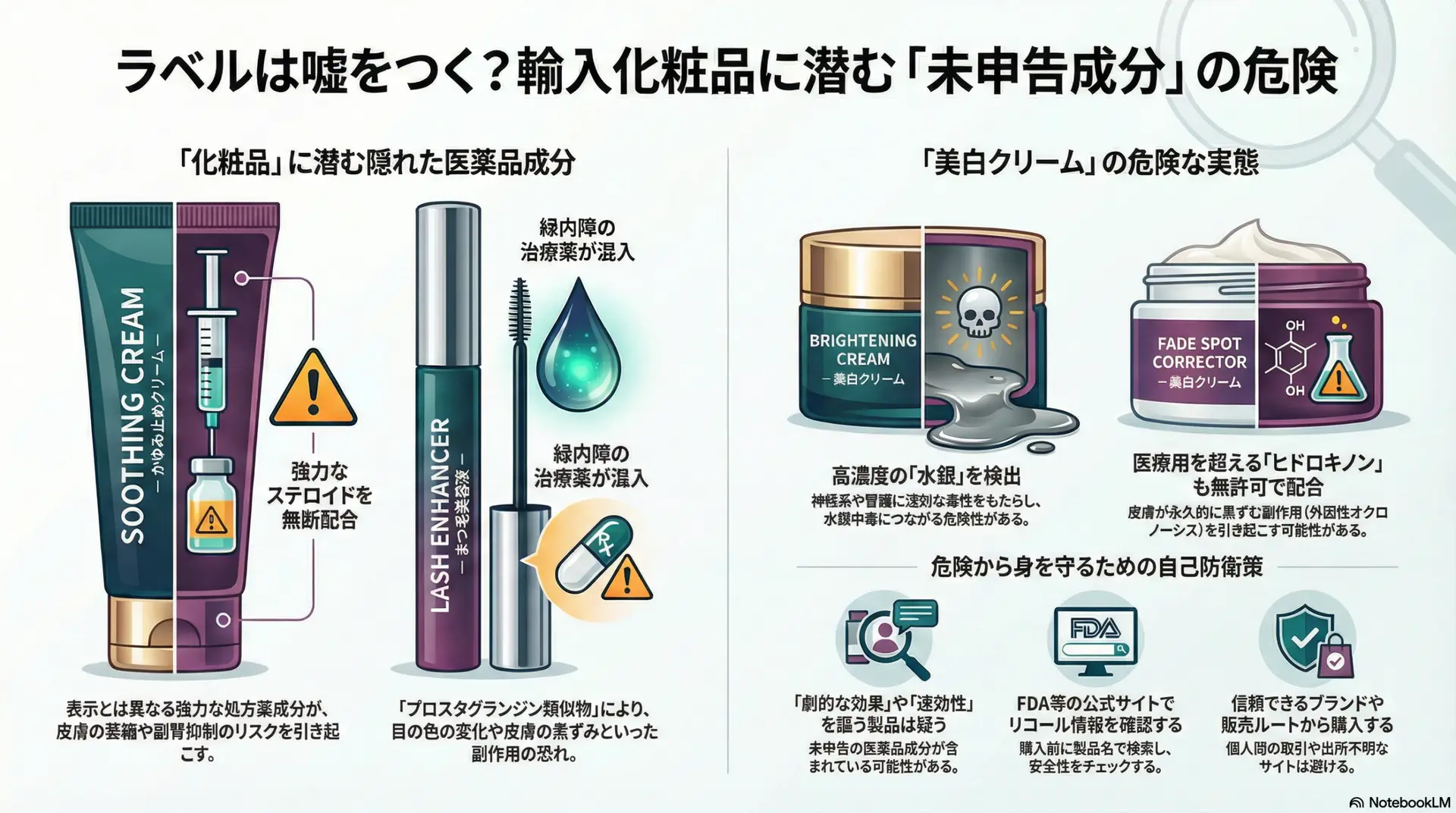
ケース1:ステロイド成分の取り違えによる重大リコール — Piyanpingかゆみ止めローション
事例の概要と発覚の経緯
2017年、米国で販売されていた中国製のかゆみ止め外用ローション「Piyanping Anti-Itch Lotion」が、表示成分と実際の配合成分が異なるとしてリコールされました。製品ラベルには「ヒドロコルチゾン1%配合」と記載されていましたが、FDA調査の結果、実際にはより強力なステロイド薬であるデキサメタゾンが含まれていたことが判明しました。
製造元は中国の広東湛江済民製薬で、米国の輸入販売元Lucky Mart社を通じて主にアジア系食料品店や漢方薬店で流通していました。FDA査察後の警告書によれば、英語と中国語の翻訳ミスにより有効成分を誤使用したことが原因とされています。
未申告成分による健康リスク
デキサメタゾンはヒドロコルチゾンと比較して作用が強力かつ持続性が長いステロイド薬です。弱いステロイドと思い込んで頻繁に塗布した場合、以下のような重篤な副作用を引き起こす可能性があります。
- 皮膚萎縮と色素脱失:皮膚が薄くなり白斑が生じる
- 副腎抑制:高血糖、免疫機能低下、電解質異常、小児の成長抑制
- 眼への影響:眼圧上昇による緑内障、白内障のリスク
FDAはこのリコールをクラスI(重大な健康被害の恐れがある状況)に分類し、当該ロットの全量回収を指示しました。
越境EC利用時の教訓
この事例は、アジア製OEM医薬部外品が米国内のエスニック市場で流通していたケースです。越境ECで外用クリームを購入する際、表示成分だけでは安全性を判断できない場合があります。特にステロイドのような医薬品成分は各国で規制が異なり、無表示で含まれている危険性があることを認識すべきでしょう。
ケース2:化粧品を装った医薬品 — Skin-Capエアロゾルスプレーの長期問題
25年以上続く未申告ステロイド問題
欧州メーカーChemigroup France製の「Skin-Cap Aerosol Spray」は、乾癬や皮膚炎のケア用途で「亜鉛ピリチオン配合」の化粧品的製品として販売されていました。しかし1990年代末にFDA試験で高力価ステロイドが密かに配合されていることが発覚し、米国・カナダ・欧州で回収措置が取られました。
問題は一度では終わりませんでした。2024年10月、FDAは再度安全性警告を発出し、オンライン販売されているSkin-Capスプレーを購入・使用しないよう呼びかけています。医学誌の報告によれば、25年以上経過した現在でも同製品からクロベタゾール等の強力なステロイドが検出され続けているとのことです。
強力ステロイドの長期使用リスク
製品から検出されたクロベタゾールなどの高力価ステロイドは、本来医師の処方のもとで短期間のみ使用される成分です。これを化粧品と誤認して長期間使用すると、以下のような全身への有害影響が懸念されます。
- 皮膚の萎縮や発疹
- 感染症リスクの増大
- 血糖値上昇や血圧変動
- 骨への障害、精神症状
- 副腎ホルモンの乱れ
FDAは使用中止を急に行うとリバウンドで症状悪化や副腎不全を起こす可能性もあるため、医療専門家への相談を強く推奨しています。
国際EC市場での流通実態
Skin-CapはAmazonやWalmartのマーケットプレイスを含む海外通販サイトで購入可能な状況でした。このように海外メーカー製の医薬品的製品が、化粧品として偽装されネット上で流通するケースは少なくありません。言語の壁による成分誤認や偽装表示に十分な警戒が必要です。
ケース3:まつ毛美容液の隠れた医薬品成分 — プロスタグランジン類似物の無表示混入
SNS流行と健康被害の裏側
近年、まつ毛美容液(ラッシュセラム)がInstagram等のSNSで流行し、劇的な育毛効果を謳う製品が人気を集めています。しかしその一部製品に、緑内障治療薬として使われるプロスタグランジンF2α類似物が無申告で配合され、大きな問題となりました。
2023年、カナダ保健省は複数のブランド(RefectoCil Lash & Brow Booster、The Ordinary Multi-Peptide Lash Serum、LiLash、EyEnvy等)について自主回収命令を発出しました。米国でもGrandeLashやRodan+Fields Lash Boostなど類似成分を含む製品が販売され、2022~2023年にかけて集団訴訟が提起されています。
検出された医療用成分とそのリスク
これらの製品から検出されたのは、ビマトプロスト、イソプロピルクロプロステネート、デヒドロラタノプロストなどのプロスタグランジン類似物です。いずれも本来は処方薬として医師の管理下でのみ使用すべき成分であり、以下のような副作用が報告されています。
- 虹彩の色素沈着(眼の色の変化)
- 眼瞼皮膚の黒ずみ
- 炎症やかゆみ、充血
- 視力の一時的低下
プロスタグランジン類似物はホルモン様作用を持ち、全身吸収の懸念もあります。米国では該当製品使用により眼の痛みや色素沈着等の被害報告が相次ぎ、製品に十分な表示・警告がなかったとしてメーカーに責任を問う訴訟が起きました。
個人輸入時の注意喚起
まつ毛美容液は海外製品を個人輸入するケースも多く見られます。しかし「劇的な効果」を謳う製品には医薬品が無表示で混入している恐れがあります。海外通販で購入する場合、その国での当局リコール情報(例えばカナダのリコール情報)を確認し、未承認成分の有無を調べることが推奨されます。
ケース4:美白クリームの危険な実態 — 水銀・ヒドロキノンの無申告配合
安価な美白効果の代償
肌の美白・シミ取りを目的としたスキンライトニング製品の中には、表示にない有害成分を含む違法品が国内外で問題となっています。特に水銀(マーキュリー)やヒドロキノンが無申告で配合されたクリームについて、FDAや各州当局が繰り返し警告・押収を行っています。
代表的な製品例としては、Crema Limpiadora y Curativa(La Tía Mana)、Carotone Black Spot Corrector、African Queen Bleaching Cream、Amos White in 7 Days等があります。多くは海外メーカー(メキシコ、パキスタン、象牙海岸など)の製品ですが、一部は米国内の業者がラベル貼り替え等で販売していたケースも存在します。
検出された有害成分の深刻度
FDA試験では、一部のクリームから数千~一万ppmを超える高濃度の水銀や、医療用を上回る4%以上のヒドロキノンが検出されています。これら成分はいずれも表示に記載されておらず、意図的に無許可で配合されていました。
水銀による健康被害:
- 神経系や腎臓への深刻な毒性
- 慢性曝露による水銀中毒(感覚障害、記憶障害、腎不全)
- 乳児への授乳を通じた母子間移行による中毒事例も報告
ヒドロキノンによる皮膚障害:
- 皮膚の永久的黒ずみ(外因性オクロノーシス)
- 重度のアレルギー性皮膚炎
2019年にはアリゾナ州でメキシコ製クリーム使用者から乳児の重度水銀中毒事故が発生し、FDAが注意喚起を行いました。また2020~2022年にかけてFDAはヒドロキノン含有OTC美白剤の販売禁止を明確化し、12社以上に警告書を発出するとともに流通在庫の回収を促しました。
密かに取引される違法美白クリーム
美白クリームは個人輸入やオークションサイト等で密かに取引されることが多く、成分偽装の温床になっています。海外では安価に劇薬成分を入れた製品も存在し、日本を含め各国で問題視されています。
FDAは「ラベルに成分未記載の場合でも、水銀や強力な薬剤が含まれるケースがある」としており、不自然に効果が高い輸入コスメは使用を控える、安全性データや当局の承認が確認できる製品を選ぶ、といった自己防衛が求められます。
MoCRAによる規制強化と今後の展望
2023年12月に施行された化粧品規制近代化法(MoCRA)により、FDAは化粧品に対する強制リコール権限を初めて持つことになりました。これにより、未申告成分混入製品に対して、企業が自発的に回収しない場合でもFDAが強制回収を命令できるようになります。
企業側もリコールを含む是正計画の策定が義務付けられ、安全な製造管理や輸入時の検査が強化される見込みです。越境ECで購入する消費者も、製品がFDAリコール対象になっていないか事前に調べることが推奨されます(FDA公式サイトのリコール情報データベースで製品名検索が可能)。
まとめ:製品表示だけに頼らない自己防衛策
本記事で紹介したFDAリコール事例からは、OEM化粧品であっても製造段階で意図せず混入・あるいは意図的に無許可成分を添加されているケースが存在することが明らかです。ステロイド、プロスタグランジン類似物、水銀、ヒドロキノンといった医薬品成分や有害物質が、消費者の知らないうちに配合されていた実態は決して軽視できません。
越境ECや個人輸入を利用する際は、以下の点に注意が必要です。
- 製品表示のみを信用せず、当局発表や試験結果を確認すること
- 異常に速効性を謳う製品には特に警戒すること
- FDA等の公式サイトでリコール・警告情報を事前にチェックすること
- 信頼できるブランドや販売ルートから購入すること
- 健康被害が疑われる場合は速やかに専門家に相談すること
化粧品の安全性は、製造者・販売者・規制当局・そして消費者自身がそれぞれの役割を果たすことで初めて守られます。本記事が、より安全な化粧品選びの一助となれば幸いです。
コメント