はじめに:Warning Letterは「最後通告」である
米国の健康食品・サプリメント業界において、FDA(米国食品医薬品局)からのWarning Letter(警告書)は、単なる「注意喚起」ではありません。過去5年間のデータを見ると、この警告を軽視した企業の多くが、ブランド崩壊、販売停止、さらには刑事訴追という深刻な事態に直面しています。
本記事では、Warning Letterへの不適切な対応により致命的な打撃を受けた6つの実例を詳しく分析します。これらの事例から、規制当局との向き合い方、コンプライアンスの本質、そして事業継続のために何が必要かを学ぶことができます。
USPlabs:業界トップブランドの完全消滅
「天然成分」という虚偽が招いた破滅
かつてスポーツサプリメント市場で圧倒的なシェアを誇ったUSPlabsは、Jack3dやOxyElite Proといったヒット商品で知られていました。しかし、その成功の裏には重大な法令違反が隠されていました。
同社の主な問題点は、未承認医薬品成分であるDMAA(1,3-ジメチルアミルアミン)を「天然由来成分」と偽って配合していたことです。安全性試験を実施せず市場に投入した結果、重篤な肝障害や死亡事例が複数報告されました。
FDAは製品リコールを命じるとともに刑事捜査を開始。2019年には経営陣が有罪答弁を行い、会社は事業停止・清算へと追い込まれました。CEOらには実刑判決が下され、かつての有名ブランドは完全に市場から姿を消しました。
この事例が示す教訓は明確です。健康被害と虚偽表示の組み合わせは、Warning Letterの段階を超えて刑事事件レベルへと発展する可能性があるということです。
Blackstone Labs:無視と隠蔽が招いた刑事責任
Warning Letterを「交渉材料」と誤解した代償
ボディビル向けサプリメントを展開していたBlackstone Labsは、2015年にFDAからWarning Letterを受け取りました。指摘されたのは、DMBA(未承認刺激物質)やSARMs(選択的アンドロゲン受容体調節薬)といった医薬品成分を、あたかもサプリメントであるかのように販売していた点です。
問題は、同社がWarning Letter受領後に取った行動にありました。表向きには販売停止を表明しながら、実際には在庫を売り切るよう指示し、販売を継続。さらにFDA調査を妨害する行為にも及びました。
この対応の結果、2019年に連邦大陪審で起訴され、2021年には会社と創業者が有罪答弁。創業者2名には約4年半の実刑判決が下され、ブランドは崩壊しました。
Warning Letterを「交渉の余地がある要求」と捉えるのは致命的な誤りです。これは規制当局からの最終的な警告であり、真摯な対応が求められます。
Enhanced Athlete:致死性物質販売でCEOに実刑
「サプリ」の名の下に危険物質を販売した末路
Enhanced Athleteは、DNP(2,4-ジニトロフェノール)という工業用化学物質を「脂肪燃焼剤」として販売していました。DNPは高い致死性を持つ物質であり、サプリメントとしての使用は極めて危険です。
同社はDNPに加えて、SARMsなどの未承認医薬品成分も多数取り扱っていました。FDAは工場を捜索し、刑事訴追へと進みます。
最終的にCEOには懲役3年の実刑判決が下され、ブランドは事実上崩壊。国際的にも「危険なブランド」として認識されるようになりました。
この事例が示すのは、製品を「サプリメント」と称して販売しても、中身が医薬品であれば法的責任を免れることはできないという原則です。
Basic Reset / Biogenyx:是正を怠り裁判所命令で事業停止
約束だけで実行しない企業の末路
健康食品とMLM(マルチレベルマーケティング)を組み合わせたビジネスモデルで展開していたBasic Reset / Biogenyxは、2016年にFDAからWarning Letterを受け取りました。
指摘内容は深刻でした。癌、糖尿病、心臓病といった疾病の治療効果を謳う表現、GMP(適正製造規範)違反、そして苦情や有害事象の管理体制が存在しないことなどです。
同社は是正を約束したものの、実際には何も実行しませんでした。この不誠実な対応に対し、2019年に連邦裁判所は永久差止命令を発出。全製品の製造・販売が禁止され、ブランドは事実上崩壊しました。
Warning Letterへの対応において、「約束」だけでは不十分です。実際の是正措置とその証明が求められます。
Golden Sunrise Nutraceutical:パンデミック便乗で一気に崩壊
COVID-19治療を謳った虚偽広告の代償
Golden Sunrise Nutraceuticalは、COVID-19のパンデミック期に、自社製品がCOVID-19、癌、パーキンソン病を治療できると宣伝しました。さらに「FDA承認済み」という虚偽表示を行い、患者に数万ドル相当の商品を販売していました。
この悪質な行為に対し、FTCとFDAは合同でWarning Letterを発出し、民事・刑事の両面から訴追を進めました。
2024年、CEOは有罪答弁を行い実刑判決を受けました。ブランドは完全に崩壊し、被害者への返金対応が行われることとなりました。
パンデミックという社会的混乱に乗じた健康強調表示は、規制当局の最優先取締対象となります。このような便乗商法は即座に厳しい措置の対象となります。
Balance of Nature:有名ブランドでも例外なし
知名度は免罪符にならない
植物系サプリメントで高い知名度を誇るBalance of Natureも、2019年にFDAからWarning Letterを受け取りました。指摘されたのは、成分検査を実施していないというGMP違反、そして癌、心臓病、COVID-19などの治療表現です。
2023年には裁判所命令により製造・販売が停止されました。同社は全面的な是正を条件に事業を再開できましたが、ブランドの信頼性には大きなダメージが残りました。
この事例が示すのは、「知名度がある企業は守られる」という考えが誤りであるということです。規制当局は企業規模や知名度に関わらず、違反があれば厳格に対処します。
Warning Letter対応の失敗パターンと教訓
破滅へのステップ
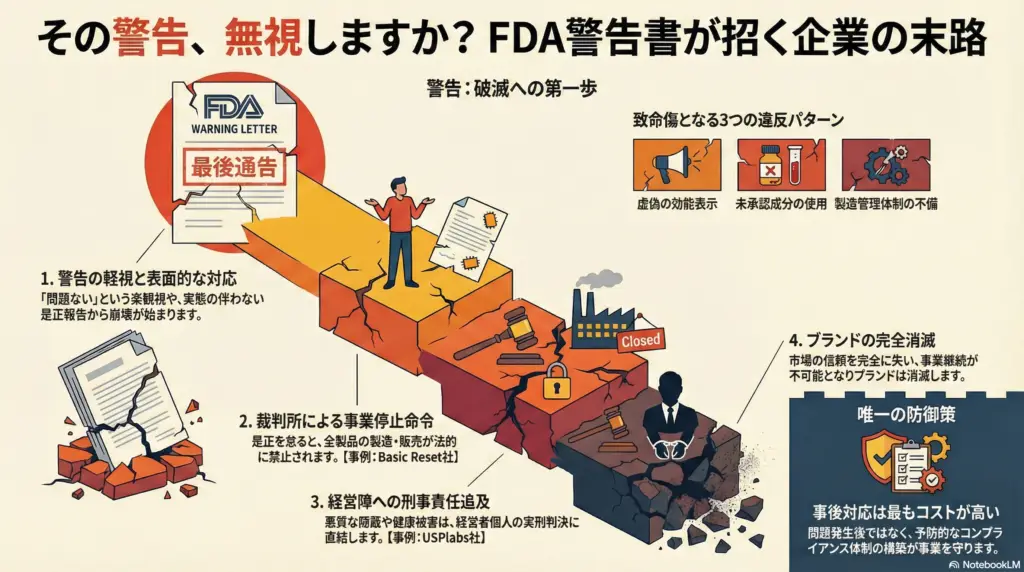
上記の事例から、Warning Letterを受けた企業が辿る典型的な破滅ルートが見えてきます。
第一段階は、Warning Letterの軽視です。「うちは大丈夫」「これまで問題なかった」という楽観的な姿勢が、最初の誤りとなります。
第二段階は、表面的な対応や是正の不十分さです。形式的な回答書を提出するだけで、実質的な改善措置を取らないケースが多く見られます。
第三段階では、FDAによる再調査や裁判所からの差止命令が発出されます。この時点で企業は大きな経済的・社会的ダメージを受けます。
第四段階は刑事・民事責任の追及です。経営陣個人が法的責任を問われ、実刑判決を受けるケースも少なくありません。
最終段階がブランドの崩壊です。市場からの信頼を完全に失い、事業継続が不可能となります。
絶対に守るべき原則
これらの事例から導き出される教訓は明確です。
まず、Warning Letterは交渉事項ではありません。規制当局からの最終警告として真摯に受け止める必要があります。
次に、健康や疾病に関する表現は最重要リスクです。治療効果を暗示する表現は、たとえ間接的であっても厳しく取り締まられます。
GMPの不備は必ず次の摘発につながります。製造管理体制の不備は、他の違反を発見されるきっかけとなります。
そして最も重要なのは、事後対応が最もコストが高いという事実です。問題が発生してから対処するよりも、予防的なコンプライアンス体制を構築する方が、はるかに効率的で経済的です。
まとめ:規制対応は事業継続の根幹
FDA Warning Letterへの対応は、単なる法令遵守の問題ではありません。それはブランドの存続、従業員の雇用、経営者の人生に直結する重大事項です。
過去5年間で崩壊した健康食品ブランドの多くは、規制を軽視し、短期的な利益を優先した結果、すべてを失いました。USPlabsやBlackstone Labsのような業界トップ企業でさえ、コンプライアンス違反によって完全消滅しています。
健康食品・サプリメント業界で事業を展開する企業には、予防的なコンプライアンス体制の構築が不可欠です。GMPの徹底、表示内容の法的レビュー、有害事象管理体制の整備など、基本的な対策を確実に実施することが、長期的な事業継続の鍵となります。
Warning Letterを受け取ってからでは遅い場合があります。今こそ、自社の製品、表示、製造体制を見直し、規制に適合した事業運営を確立すべき時です。
コメント