米国向けに食品を輸出する日本企業にとって、FSMA(Food Safety Modernization Act:米国食品安全強化法)への対応は避けて通れない課題となっています。2011年の制定以降、FSMAは食品安全管理の重点を事後対応から事前予防へと大きく転換させ、2024年現在では本格的な執行段階に入っています。
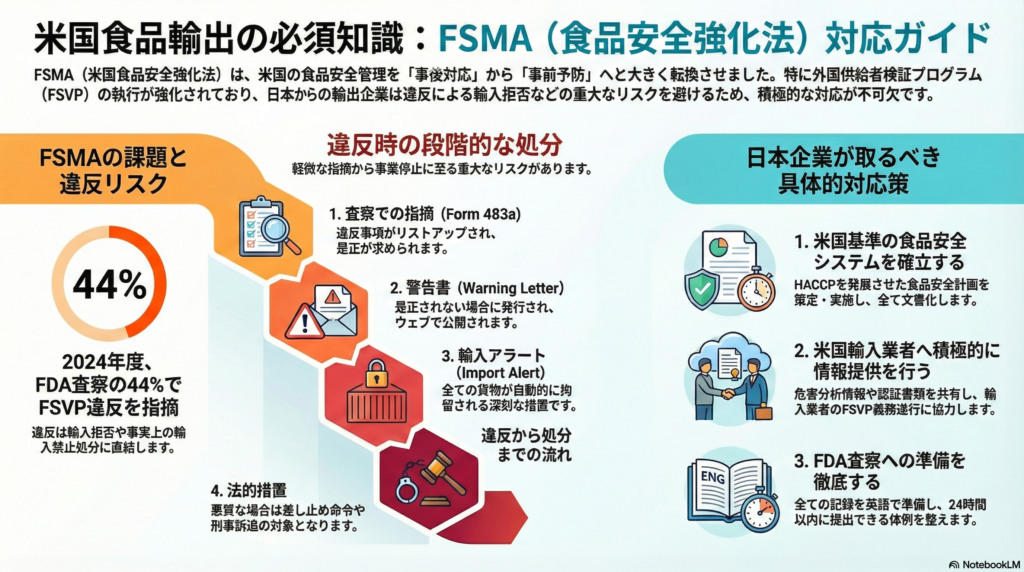
特に注目すべきは、2024年度のFDA査察において全輸入業者査察の約44%でFSVP(外国供給者検証プログラム)違反が指摘され、38通もの警告書が発出されたという事実です。これは単なる書類上の問題ではなく、違反企業には輸入拒否や事実上の輸入禁止処分といった深刻な結果が待ち受けています。
本記事では、FSMAの最新要求事項から実務対応まで、日本企業が米国市場で安定したビジネスを継続するために必要な知識を包括的に解説します。
FSMAの基本構造と2024年最新動向
FSMAが求める7つの主要規則
FSMAは包括的な食品安全法として、以下7つの主要規則を定めています。
人用食品および動物用食品の予防的管理策では、製造施設にハザード分析と予防管理計画の策定・実施が義務付けられます。生鮮農産物の安全基準は、農場での栽培・収穫段階における衛生管理を規定します。輸入食品の外国供給者検証プログラムは、米国輸入業者に対し外国サプライヤーの検証を求めるものです。
食品のトレーサビリティ規則は特定のハイリスク食品に追加の記録管理を義務付け、当初2026年1月施行予定でしたが2028年7月まで猶予されています。食品防御規則は意図的な異物混入への対策を、認定第三者監査制度は海外施設の監査体制を、そして自発的品質輸入者プログラムは優良輸入業者への優遇措置をそれぞれ定めています。
2024年における執行強化の実態
これらの規則は2016年から2018年にかけて順次施行され、中小事業者への適用猶予も概ね終了しました。現在は本格的な執行段階にあり、FDA(米国食品医薬品局)は違反に対する取締りを強化しています。
2024年度の査察データが示す通り、特にFSVP未整備が最も多い違反事例となっており、警告書の約4割は生鮮農産物の輸入業者に対するものでした。この傾向は、サプライチェーン全体での食品安全管理強化というFSMAの方向性を如実に表しています。
FSVP(外国供給者検証プログラム)の実務要件
FSVPインポーターの役割と責任
FSVPはFSMAの中核規則として、米国の食品輸入業者に外国サプライヤーが米国内生産者と同等の食品安全基準を満たしていることの検証を義務付けています。具体的には、輸入食品が米国のハザード分析・予防的管理基準または生鮮農産物安全基準に照らして同等の公衆衛生保護水準で生産されていること、不良品でないこと、誤表示がないことを確認する必要があります。
FSVPインポーターは原則として米国に拠点を持つ事業者でなければなりません。輸入時点で食品の所有者または荷受人となる米国内の事業者が該当し、該当者がいない場合は外国サプライヤーが米国在住の代理人を指名し、税関に届け出る必要があります。
危害分析とリスク評価のプロセス
FSVP計画の策定は、まず輸入食品について生物学的・化学的・物理的危害要因を洗い出すことから始まります。放射性物質やアレルゲンを含む化学的危害、病原菌などの生物学的危害、金属片などの物理的危害について、既知または合理的に予見可能なものを特定します。
この際、食品の製造工程、原材料、包装、保管流通状況、最終消費形態など様々な要因を考慮し、管理策が無い場合の発生確率と影響の深刻度を評価します。輸入業者自らが分析を行うか、第三者による分析結果を取り寄せてレビュー・評価することで対応可能です。
次に、危害分析に基づき当該食品と外国サプライヤーがもたらすリスクの総合評価を実施します。食品中の危害の性質と管理主体、外国サプライヤーの食品安全手続きや設備、FDA関連規制への適合状況、過去の違反・リコール歴や問題発生時の対応状況などを総合的に評価し、そのサプライヤーを承認してよいかを判断します。
供給者検証活動の具体的手法
承認した各外国サプライヤーについては、リスク評価に応じた適切な検証を実施する必要があります。検証方法には柔軟性がありますが、SAHCODHA(人または動物に深刻な有害健康影響または死亡をもたらし得る重大危害)が懸念される食品の場合、原則として年次の現地監査を実施しなければなりません。
具体的な検証手段としては、サプライヤー施設のオンサイト監査、輸入食品の抜き取り試験検査、サプライヤーの食品安全記録の入手・レビューなどがあります。これらの検証活動は輸入業者自身が実施するのが原則ですが、第三者に代行させることも可能です。ただし外国サプライヤー本人やその従業員は自社の検証を自ら行うことは認められず、第三者による場合でも輸入業者がその結果記録を入手し内容を評価・保持する必要があります。
是正措置と継続的改善
検証の結果、外国サプライヤーが適切な安全管理を実施していない、または輸入食品が基準を満たさず不適格であることが判明した場合、輸入業者は速やかに是正措置を講じなければなりません。
是正措置の内容は状況によりますが、問題の原因が解決され適合が確認されるまで当該サプライヤーからの調達を中止する、一時的に検査頻度を上げる、サプライヤーと改善計画を策定するといった対応が考えられます。是正措置を講じた場合も、その内容と効果を記録として残し、必要に応じFSVP計画を更新します。
サプライチェーン管理における記録保持義務
文書化の重要性と保存期間
FSMAでは「文書化されていないことは、起こらなかったことと同じ」との考え方が取られており、徹底した記録保持がコンプライアンスの基本となります。
危害分析の結果レビュー、供給者の評価結果、実施した検証活動の内容・日付・結果、是正措置の内容など、FSVPに関するあらゆる事項を漏れなく文書化し、少なくとも2年間保存する必要があります。記録は原本または真正なコピーで判読可能な状態で保管し、紙・電子いずれの形式でも構いません。
FSVP計画の定期見直しと更新
輸入業者はFSVPを最低3年ごとに再評価し、新たな情報があれば適宜計画をアップデートすることが求められます。新規の危害や法規制の変更、サプライヤーの状況変化などは見逃さず、記録に反映するとともに、必要なら検証活動やリスク評価をやり直します。
サプライヤーの製造工程変更や新製品の追加なども重要な更新トリガーとなります。定期的な内部監査や文書見直しによってFSVP計画が最新の規制要求および現状に合致しているか確認することが推奨されます。
FDA査察への実践的準備
査察通知から実施までの流れ
FDAは通常、FSVP査察を行う際に事前に輸入業者へ連絡を入れますが、通知期間は長くなく、1週間程度前に予告されるケースも多いと報告されています。査察は主に書類審査の形で行われ、FDA調査官はFSVP記録を確認し、必要に応じて質疑応答や現場確認を通じて規則遵守状況を判断します。
英語記録の整備と24時間ルール
記録は原則として英語で用意しなければなりません。社内で他言語で作成している場合は、査察時に速やかに英訳を提出できるよう備えておく必要があります。FDAから記録提出を求められた場合、オフサイトに保管している記録も24時間以内に取り寄せて提示できなければなりません。
FDAは事前連絡の際に記録が英語で用意されているか確認してくるため、翻訳が必要な記録は査察日までに英訳を用意しておくことが推奨されています。食品仕様書や工程フローチャート、HACCP計画、検証結果報告書などは予め英語版を用意するか、少なくとも主要部分を英訳した文書を揃えておくべきです。
査察対応の体制構築
FSVPの作成・運用を担当する「適格な個人」を特定し、査察時にはその担当者または十分に事情を知る責任者が立ち会えるよう調整します。FDAは査察時に、FSVP作成維持責任者と直接議論したり説明を受けたりすることを希望するため、担当者不在の場合でも電話参加などでリアルタイムに対応できる体制を用意しておくべきです。
社内で英語対応ができるスタッフや翻訳者を確保し、調査官からの質問や追加資料要求に迅速に答えられるよう訓練しておくことも有用です。査察中は調査官との積極的なコミュニケーションが推奨されており、疑問点にはその場で回答・討議し、可能な是正は即時に行う姿勢を示すことが重要です。
電子記録提出への対応
FDAは近年、FSVP記録を電子的に提出させる仕組みも整備しています。実際、FDAはFSVP記録提出用の「インポーター・ポータル」を開設しており、査察に先立って記録の電子提出を求められる場合もあります。ポータル経由の提出要請があった場合に迅速に対応できるよう、PDF化やデータ整理をしておくとよいでしょう。
違反時のリスクと段階的な処分
輸入拒否と通関保留
FSVP要件を満たしていない食品は米国への輸入を拒否される可能性があります。税関での書類審査等において「適切なFSVPが実施されていない」と判断されると、その食品は不合格品と見做され米国内に搬入できません。
実務上も、FDAが輸入業者にFSVP記録の提出を求め、提出できなかった場合にそのロットの通関が保留・拒否されるケースがあります。これは他の違反と同様、輸入時点で適用される厳しい措置です。
査察所見(Form FDA 483a)と是正期間
FDAのFSVP査察で違反が見つかった場合、まず調査官はForm FDA 483aにより違反事項をリストアップし、企業に指摘します。指摘内容には、不足しているFSVP要素が具体的に挙げられます。
指摘を受けた輸入業者は、是正計画を迅速に策定し、可能であれば15営業日以内にFDAへ改善措置を文書で報告することが望まれます。これは公式な期限ではありませんが、警告書回避のための目安となります。
警告書の発行と公開
初回の指摘に対し適切な是正措置が取られなかったり、追査で依然としてFSVP違反が認められたりした場合、FDAは対象業者に対し公式の警告書を発行します。警告書では、該当業者がFD&C Act 805条に違反していることが法的に指摘され、速やかな是正が求められます。
警告書はFDAのウェブサイト上で一般公開されるため、企業の信用失墜や取引先への悪影響も大きく、警告書を受けること自体が大きなリスクです。2024年度にはFSVP違反で38通の警告書が発行されており、その内容は大半が「適切なFSVP計画を有していない」という基本的事項でした。
輸入アラートと自動拘留
警告書受領後も問題が改善されない場合、FDAは当該輸入業者を輸入アラートリストに掲載し、以後その業者が関与する食品の輸入を自動的に拘留の対象とする措置を取ります。
輸入アラート99-41号「FSVP不履行の輸入者による食品の拘留」リストに掲載されると、当該業者が輸入しようとする全ての食品が原則検疫所でストップされ、物理的な検査なしで通関不許可となります。この状態から脱却するには、FDAに対し是正措置を講じた証拠書類を添えて解除申請を行い、承認を得る必要があります。解除手続には通常数ヶ月を要し、その間ビジネスに大きな支障が生じます。
その他の法的措置
悪質な違反や重大な食品安全事故に繋がる場合、FSMA違反は差し止め命令や刑事訴追の対象ともなりえます。FSMAではFDAに強制的なリコール命令権限や、施設登録の一時停止権限も付与されています。
また、FSVP違反を放置したまま営業を続けることは米国市場での信用を喪失し、取引先から取引停止や契約解除に至るリスクもあります。民事上も、流通先や消費者から訴訟を提起されるリスクが高まる可能性があります。
日本企業が取るべき具体的対応策
FSMA規則への包括的対応
自社が米国向けに輸出している食品がFSMAのどの規則の影響を受けるかを把握しましょう。製造施設として米FDAの登録義務があり、2年ごとの更新が必要です。人用食品を製造している場合はFSMA第103条の予防的コントロール規則が求められ、現行のHACCPを発展させた食品安全計画の策定・実施が必要となります。
さらに売上規模等によっては食品防御計画の策定も必要です。自社が該当するFSMA要件を洗い出し、必要な対策を講じていることを確認してください。未対応の場合は専門家の支援も検討すべきです。
食品安全マネジメントシステムの確立
米国の基準に見合う食品安全マネジメントシステムを社内に確立する必要があります。HACCPやISO 22000、FSSC 22000などの認証取得や、米国の予防管理規則に対応した食品安全計画を策定・実施することが望ましいでしょう。
製造工程でのCCP管理、アレルゲン管理、サプライヤー原料管理、製品検査などを含む包括的な安全対策を講じ、その内容と結果をすべて文書化しておきます。監査時に提出できる記録類を整備してください。
米国輸入業者への積極的な情報提供
自社製品の米国インポーターに対し、FSVP義務を円滑に果たせるよう必要な情報提供と協力を行いましょう。製品ごとの危害分析情報や製造工程フロー、使用原料リスト、各種検査結果、認証書類があれば事前に共有します。
自社が実施しているHACCPや予防的コントロールの内容をまとめた英文の説明資料を用意し、供給者としてどのような安全管理を行っているか明示すると、輸入業者の評価作業が大いに助かります。現地監査を要請された場合には、必要な準備を整え、誠実に対応してください。
第三者認証とVQIPの活用
自社の食品安全システムに対する第三者認証取得を検討してください。FDAはFSMAに基づき認定第三者監査制度を導入しており、海外施設がFDA公認の認証機関による監査証明を取得すると、輸入業者向けの自発的品質輸入者プログラムへの参加要件を満たすことができます。
VQIPに参加した輸入業者は当該食品の迅速通関や検査の優遇措置を受けられるため、結果的に輸出企業にとってもメリットがあります。検査頻度の大幅減や通関遅延リスクの低減といった恩恵が得られ、ビジネス上の競争力向上につながります。
トレーサビリティシステムの整備
商品ロットの追跡情報を迅速に提供できるトレーサビリティシステムを導入することも有益です。特定のハイリスク食品に対するトレーサビリティ規則は2028年7月まで施行が猶予されていますが、早期の準備により将来的なリスク低減に直結します。
輸出国ごとに異なる規制要求をリスト化し管理する仕組みを整える、重要追跡イベントとキー・データ要素の記録体制を構築するといった取り組みが推奨されます。
まとめ:コンプライアンス文化の醸成と継続的改善
FSMA対応は一過性の対応ではなく継続的な改善活動です。社内に食品安全と法令順守の文化を根付かせ、経営層から現場まで一丸となって取り組むことが求められます。
米国向けのみならず、他国向け輸出や国内市場においても食品安全基準は年々高度化しています。FSMAへの対応を契機に、自社のサプライチェーン全体を再点検し、弱点を補強することは将来的なリスク低減に直結します。
「自社製品が米国法規を100%満たしている」と胸を張って言える状態を作るために、必要な社内体制整備や文書作成、人材育成に投資し、米国の輸入業者と協調しながらFSMAコンプライアンスを実現することが、安定した対米輸出ビジネスの鍵となります。
FDAや信頼できる情報源から最新動向を入手し、プロアクティブに対応していくことで、警告書や輸入拒否といったリスクを未然に防ぎ、米国市場での競争優位性を確保することが可能となるでしょう。
コメント