はじめに:CBPを「関税を取る機関」と思っていると痛い目を見る
米国へ商品を輸出したことのある方なら、一度は「通関で止まった」という経験や話を耳にしたことがあるかもしれない。しかし、なぜ止まったのか、どうすれば止まらないのかを深く理解できている人は意外と少ない。
その背景には「CBP(米国税関・国境警備局)は関税を取るだけの機関」という根強い誤解がある。実際にはCBPは、貨物が米国内に入る際の申告内容の正確性から法令・規制の遵守まで、幅広い観点で確認を行う機関だ。
この記事では、CBPが実際に何を見ているのかを整理し、通関トラブルを未然に防ぐための実務的な視点を提供する。特にFDA規制が絡む食品・サプリ・化粧品・ウェルネス系商品を扱う方にとっては、見落とせない内容が含まれている。
CBPの役割:関税だけではない「4つの審査軸」
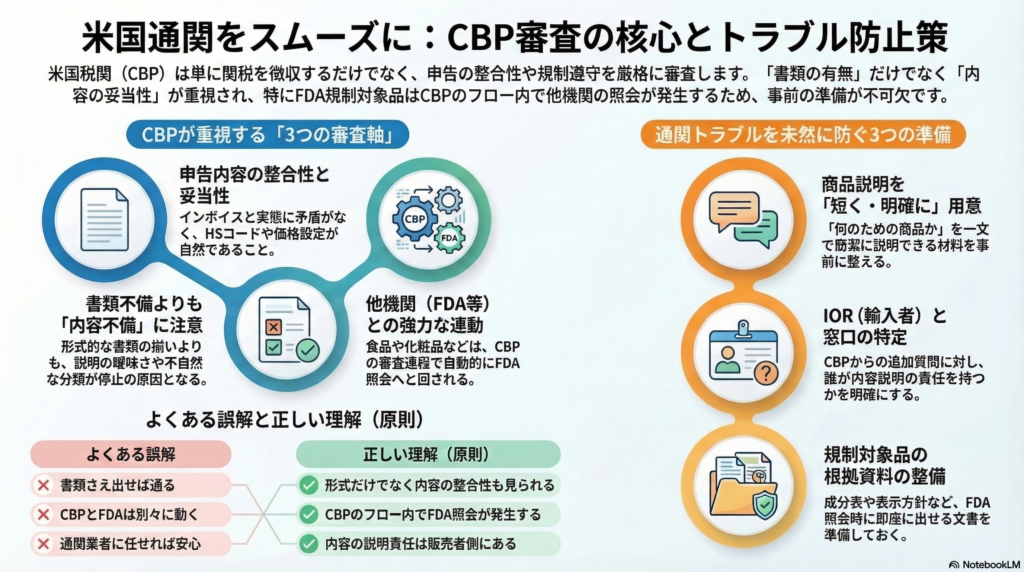
CBPが実際に確認していること
CBPが輸入貨物に対して確認するポイントは、大きく4つの軸に整理できる。
① 申告の整合性 提出された書類の情報が揃っているか、矛盾していないかを確認する。インボイス・パッキングリスト・出荷情報の間で品名・数量・価格が一致していることが前提となる。
② 分類・課税の妥当性 その商品がどの品目分類(HSコード)に該当するか、それに基づく関税・税金の前提が適切かを見る。分類が不自然に見える場合は追加確認の対象になる可能性がある。
③ 内容の妥当性 品名・用途説明・数量・価格が現実と噛み合っているかどうか。「書類が揃っている」だけでは不十分で、説明が実態と一致していることが求められる。
④ 規制対象の可能性 特定のカテゴリ(例:食品・医薬品・化粧品)に該当する可能性がある場合、FDA等の別機関への照会が必要になることがある。
この4軸を理解しておくだけで、通関トラブルの多くが「事前に防げるもの」として見えてくるようになる。
「書類不備」と「内容不備」は止まり方が違う
通関が止まる2種類の原因
通関が止まる原因は大きく2種類に分類できる。
書類不備とは、必要な情報が足りない、あるいは書類の形式や記載が揃っていない状態を指す。たとえばインボイスに必須項目が記載されていなかったり、パッキングリストが添付されていなかったりといったケースがこれに当たる。
内容不備とは、説明が曖昧であったり、分類が不自然であったり、書類間または実態との間に矛盾がある状態だ。書類が「形式上は揃っている」ように見えても、内容の整合が取れていなければ問題になりうる。
止まり方の段階的プロセス
通関が止まる流れは、おおむね以下のように段階的に進むと考えると理解しやすい。
- 自動チェックで引っかかる:情報の不整合・不足がシステム上で検出される
- 人の確認対象になる:追加説明や現物検査が求められる
- 別機関照会に回る:必要に応じてFDA等に照会が発生する
この段階を把握しておくと、「止まってから対応する」ではなく「止まらないように準備する」という発想に切り替えやすくなる。
実務でよく起きる通関停止のパターン
通関が止まりやすい6つの原因
① 品名・用途説明が曖昧
「何のための商品か」が短く明確に説明できない場合、CBPが追加確認を求めやすい。特に新しいカテゴリの商品や、複数用途が考えられる商品では、用途説明の明確さが通関の通りやすさに直結する。
② 書類間の不一致
インボイス・パッキングリスト・出荷情報のいずれかで数量・品名・価格が噛み合っていない場合、整合性のチェックに引っかかりやすい。出荷前の最終確認で防げるケースが多い。
③ 分類(品目)や価格が不自然
申告内容が実態とズレているように見えると、確認が入る可能性が高まる。過去に類似商品で問題があったカテゴリでは、特に丁寧な説明が求められることがある。
H3:④ 輸入者(IOR)や窓口が曖昧
追加質問が届いても「誰が答えるのか」が決まっていない状態では、返答が遅れて長引きやすい。通関業者がいても、商品内容の詳細は販売者側でしか答えられないことが多い。
⑤ FDA等の規制照会が入るケース
食品・サプリメント・化粧品・ウェルネス系の商品は、用途説明や表現とFDA規制との整合が弱いと照会対応で時間が伸びやすい。「FDAとCBPは別」と思い込んでいると、CBPの通関フロー内でFDA照会が発生することを見落としやすい。
⑥ 通関業者任せで販売者側の情報が出せない
通関業者が手続きを進めても、商品内容の説明は販売者側の情報が必要になる場面がある。通関業者はあくまで「手続きの代理」であり、「内容の説明責任」は販売者側にある。この区別を曖昧にしておくと、いざというときに対応できない。
CBPとFDAの連動:規制対象商品の落とし穴
「CBPはCBP、FDAはFDA」という誤解が危険な理由
日本からの輸出者がしばしば持つ誤解の一つが、「CBPとFDAは別々に動いている」というものだ。実際には、CBPの審査プロセスの中で、規制対象の可能性がある商品に対してFDA照会が行われる仕組みが存在する。
つまり、FDAへの事前対応が不十分なまま出荷すると、CBPの通関フローの中でFDA照会が発生し、結果として通関全体が長期化する可能性がある。
FDA照会が起きやすい商品カテゴリ
以下のカテゴリは特に注意が必要とされやすい。
- 食品・飲料(機能性を示唆する表現があるもの)
- サプリメント・栄養補助食品
- 化粧品・スキンケア製品
- ウェルネス系・健康関連商品
これらは用途説明・ラベル表記・成分情報がFDA規制と整合していないと、照会対応に相当な時間を要することがある。
事前に準備すべき「説明材料」
照会が来たときに慌てないために、以下の材料を事前に整えておくことが有効な可能性がある。
- 用途説明(何のための商品か、明確かつ簡潔に)
- 表示方針(ラベルにどのような主張・表現を使っているか)
- 成分・仕様情報(成分リスト、配合比率など)
- 安全性に関する文書(必要に応じて)
よくある誤解と正しい理解の対比
誤解を一つずつ解消する
通関に関する誤解は、実務上のトラブルに直結しやすい。ここでは代表的な誤解と、それに対する正しい理解を整理する。
| よくある誤解 | 正しい理解(原則ベース) |
|---|---|
| 「書類さえ出せば通る」 | 書類の形式だけでなく、内容の整合性も見られる |
| 「止まったら運。基準は分からない」 | 止まりやすい原因は書類不備・内容不整合・窓口不明に集約されやすい |
| 「CBPとFDAは別々に動いている」 | CBPの通関フロー内でFDA照会が発生することがある |
| 「通関業者がいれば安心」 | 手続き代理と内容説明責任は別。販売者側の情報提供が必要になることがある |
| 「止まった=違法なことをした」 | 情報不足・説明不十分でも止まることはある |
事前に知っていれば防げる:通関トラブルへの備え
出荷前にできる4つの準備
通関トラブルの多くは、出荷前の準備によって防げる可能性がある。以下の4点を事前に確認しておくことで、リスクを下げやすくなる。
① 申告内容と実態の整合確認 品名・用途・数量・価格が書類間で揃っているかを出荷前に確認する習慣をつける。
② IOR(輸入者)と対応窓口の事前設定 追加確認が来たときに誰が答えるのかを、出荷前に明確にしておく。
③ 用途説明を「短く・明確に」準備する 「この商品は何のためのもので、どのように使うのか」を一文で説明できるようにしておく。
④ FDA該当の可能性があれば説明材料を整える 照会が来てから「証明書はどこだ」と探し始めるのではなく、事前に文書を揃えておく。
まとめ:CBPを「ブラックボックス」にしない
この記事のポイントと次に知るべきこと
CBPは「関税を取るだけ」の機関ではない。申告の整合性・内容の妥当性・規制対応の可能性という複数の観点から貨物を審査する機関だ。
この記事で理解しておくべき核心は3点に絞られる。
- CBPは「書類があるか」だけでなく「申告が筋の通っているか(整合性)」を見やすい
- 止まりやすい原因は、書類不備・内容不整合・窓口不明に集約されやすい
- 規制対象の可能性がある商品では、CBPの通関フロー内でFDA照会が起き得る
CBPの仕組みを「ブラックボックス」として業者任せにするのではなく、輸出者・販売者自身が基本構造を理解しておくことが、中長期的に安定した輸出体制をつくる上で重要な可能性がある。
コメント