はじめに|「止まった」は終わりではない。正しく切り分ければ動き出す
米国向け輸入ビジネスを進めているとき、ある日突然「荷物が届かない」「通関が止まっている」という状況に直面することがある。そのときに感じる不安は当然だが、止まること自体は制度上あり得ることであり、正しく対処すれば多くのケースで解決できる。
問題になるのは、「止まった=違法なことをした」「急いで何かを変えなければ」と焦って動くことだ。実際には、焦りによる無計画な修正が事態を悪化させるケースは少なくない。
この記事では、通関が止まったときに最初にやるべき原因の切り分け、書類不備と内容不整合の違い、通関業者・FDA照会への対応方法、そして再発を防ぐ記録の整理まで、実務の流れに沿って解説する。
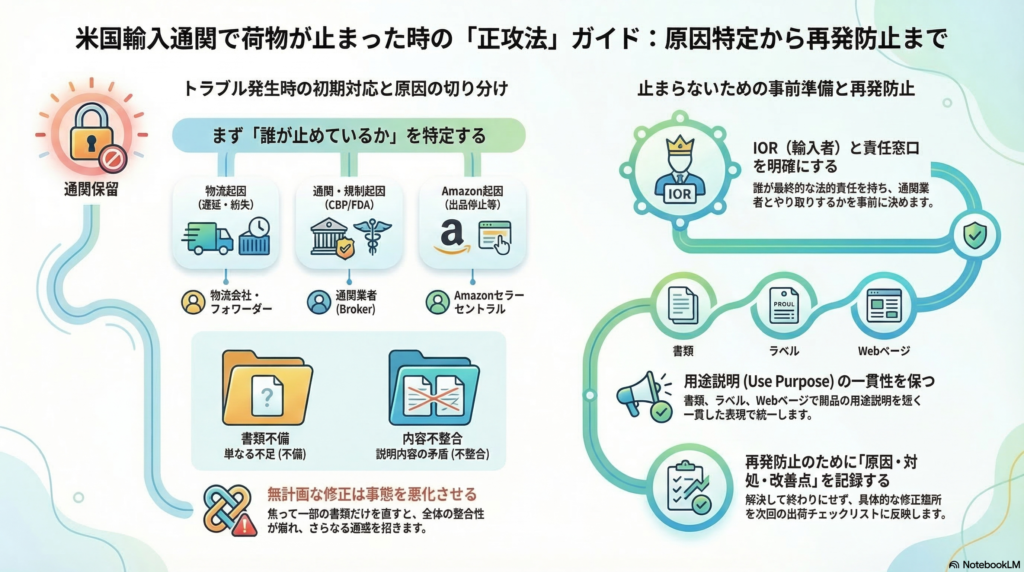
止まったときに最初にやること|「誰が止めているか」を特定する
原因は1つではないことが多い
通関が止まったとき、多くの人が「通関業者に任せているから大丈夫」「Amazonに連絡すれば解決する」と思いがちだ。しかし、輸入にかかわる関係者は複数存在し、誰が何を止めているかを最初に明確にしないと、窓口を誤って時間を無駄にしてしまう。
一般的に、止まる原因は以下の4つに大別できる。
① 物流起因
- 運送遅延・紛失・破損など
- 連絡先:物流会社・フォワーダー
② 通関起因(CBP:米国税関・国境警備局)
- 書類不備、内容不整合、追加確認
- 連絡先:通関業者経由でCBPへ対応
③ 規制照会(FDAなど)
- 規制対象の可能性がある商品への確認
- 連絡先:通関業者経由で必要な説明資料を準備
④ Amazon起因
- 出品停止、書類要求、表現修正など
- ※輸入・通関とは別の問題。対応先はAmazonセラーセントラル
この4つを最初に切り分けることが、対処の第一歩となる。物流会社に通関の問題を聞いても解決しないし、Amazonに連絡しても税関は動かない。窓口の特定が解決の速度を大きく左右する。
通関停止の2大パターン|「書類不備」と「内容不整合」は別物
書類不備とは何か
書類不備とは、必要な書類が揃っていない、または形式や数字に不一致がある状態を指す。例えば、インボイスと船積書類の金額や数量が一致していない、必要な認証書類が添付されていないといったケースが該当する。
書類不備の場合、不足・不一致を解消する書類を揃えて提出することが対処の基本となる。
内容不整合とは何か
内容不整合は、書類が揃っていても用途説明が曖昧、分類が不自然、書類と実態が噛み合っていない状態を指す。
例えば、商品の用途説明がHSコードの分類と矛盾している場合や、製品の成分・仕様の記載が実物と異なる場合がこれにあたる。この場合、追加書類を送っても、用途説明や整合性が弱いままでは解決しないことが多い。
両者を混同すると対応が長期化する
「書類を増やせばなんとかなる」と思い込んで、用途説明や整合性の問題を放置すると、追加書類が逆に疑問を増やすこともある。「何が足りないのか(書類不備)」と「何が矛盾しているのか(内容不整合)」を分けて考えることが重要だ。
焦って動くと悪化するリスク|よくあるNG行動と注意点
無計画に書類・商品ページを修正する
通関が止まったと知った瞬間、「何か直さなければ」と思い、商品ページの表現や書類を無計画に変更してしまうケースがある。しかし、書類間の整合性がさらに崩れる可能性があり、事態が悪化することもある。
修正を行う場合は、必ず「何が問題か」を特定した上で、関連する書類全体の整合性を保ちながら修正することが重要だ。
通関業者に丸投げして待つだけになる
通関業者はCBPとの交渉窓口になれるが、商品に関する情報(用途説明・成分・仕様など)は販売者側が提供しなければならない。 通関業者が「用途を説明してほしい」「この成分の詳細を教えてほしい」と求めてきたときに、販売者側が答えられないと手続きが止まってしまう。
「通関業者に任せているから自分は関与しなくていい」という考え方は、対応の遅延につながる誤解だ。
「原因は1つで、すぐ特定できる」と思い込む
通関停止の原因は、複数が重なっているケースもある。書類不備と内容不整合が同時に発生していたり、物流の問題と通関の問題が混在していることもある。「1つ直せばすぐ解決する」という前提を持つと、対応が短絡的になりやすいため注意が必要だ。
FDA照会が入ったときの対応方法
FDAが関係する可能性があるカテゴリとは
食品・飲料、化粧品・スキンケア、医療機器に準ずるもの、サプリメント類など、一部のカテゴリでは通関の流れの中でFDA(米国食品医薬品局)による照会が入る可能性がある。これは違反を意味するものではなく、制度上の確認プロセスの一部として起こり得る。
FDA照会で求められる説明材料
FDA照会が入ったときに重要になるのが、以下の3点の整合性だ。
- 用途説明(Use Purpose):この商品は何のためのものか、一貫した短い説明
- 成分・仕様(Ingredients / Specifications):原材料・成分・規格の詳細
- 表示方針(Labeling Policy):ラベル・商品ページでの訴求表現との整合
この3点が整理されていないと、照会への回答が遅れ、長期化する可能性がある。逆に言えば、出荷前にこれらを整理しておくことが、照会が入っても短期間で対応できる準備になる。
「答えられない」で長引くケースを減らすには
FDA照会が入った際に、販売者側が「成分の詳細が手元にない」「用途を一言で説明できない」という状態だと、回答が遅れ照会が長期化しやすい。
出荷前に、商品ごとに用途説明・成分一覧・表示方針をまとめた資料を1枚でも用意しておくことが、実務上の保険として機能する。
IOR(輸入者)と責任窓口を先に決めておく重要性
IORとは何か
IOR(Importer of Record)とは、輸入の際に通関申告の法的責任を持つ者のことだ。アメリカへの輸入においては、誰がIORになるかによって、税関対応の責任主体が変わる。
IORが曖昧だと対応が止まる
「誰が最終責任を持つか」が不明確な状態だと、通関業者からの質問が届いても、誰が回答すべきかがわからず対応が止まるケースがある。販売者・物流会社・通関業者のそれぞれが「相手がやるはず」と思い込んでいると、誰も動かない状態が生まれやすい。
事前にIORと通関業者への連絡窓口を明確にしておくことで、止まったときの対応スピードが大きく変わる。
再発防止に欠かせない「原因の記録」
なぜ記録が必要か
通関が止まった理由とその対処内容を記録していないと、次の出荷で同じ場所で止まる可能性が高い。「なんとか解決した」で終わらせてしまうと、同じ申告・同じ書類・同じ用途説明で繰り返すことになりやすい。
記録に残すべき4つのポイント
① 何が原因だったか(書類不備 or 内容不整合 or 物流 or FDA照会) ② どこに問題があったか(具体的な書類・記載箇所・説明内容) ③ どう対処したか(追加提出した書類・修正した説明など) ④ 次回の出荷で変えるべき点(書類フォーマット・用途説明の文言など)
この4点を、商品単位または出荷単位で簡単にまとめておくだけで、次回の対応精度が格段に上がる。チェックリストに組み込むことで、出荷前の見直しにも活用できる。
出荷前に整えておくべき3つの準備
用途説明の「短く一貫した言語化」
商品の用途を一言で説明できるように、あらかじめ整理しておくことが重要だ。「このサプリメントは何のためのものか」「この美容機器の用途は何か」を、書類・ラベル・商品ページで一貫した表現で使えるようにしておく。
書類間の整合性チェック
インボイス・パッキングリスト・製品仕様書など、複数の書類間で数量・金額・品名・用途の記載が一致しているかを出荷前に確認しておくと、書類不備による通関停止を減らせる可能性がある。
IORと通関業者窓口の事前確定
誰がIORを担当し、通関業者へのコンタクト窓口が誰なのかを出荷前に明確にしておく。これにより、止まったときの追加確認への即応が可能になる。
まとめ|「止まったときの型」を持つことが最大の対策
通関で止まったときに大切なのは、パニックで動き出す前に「誰が止めているか」を切り分けることだ。物流・CBP・FDA・Amazonの4つのどこに原因があるかで、対応の窓口も方法もまったく異なる。
また、通関停止には「書類不備」と「内容不整合」という2つのパターンがあり、混同すると対処がすれ違いになりやすい。書類を増やすだけでなく、用途説明の整合性も同時に確認することが重要だ。
さらに、出荷前の準備が「止まりにくくする」最大の保険になる。用途説明の言語化、書類整合チェック、IORと窓口の確定を事前に整えておくことで、問題が起きたときの対応スピードも大きく変わる。
通関で止まること自体は制度上起こり得ることだ。しかし、正しい型を持っていれば、焦ることなく、必要な情報を揃えて前に進める。
コメント