ビタミンサプリメントの健康強調表示リコールが急増する背景
米国ではビタミンを含む栄養補助食品市場が年間500億ドル規模に成長する一方で、科学的根拠のない健康強調表示によるFDA規制違反が後を絶ちません。特にパンデミック以降、感染症予防や疾病治療を謳う違法表示製品に対する取締りが強化されており、企業にとって表示コンプライアンスの重要性が増しています。
本記事では実際のリコール事例を通じて、どのような表示が違法とされるのか、FDAがどのように対応するのか、そして企業が負うべき法的責任について詳しく見ていきます。
COVID-19効能表示によるリコール事例の詳細分析
Golden Nutrition社の自主回収に至る経緯
2020年6月、フロリダ州のGolden Nutrition Inc.は「Anti-Viral Immune Enhancement Capsules」の自主リコールを実施しました。この製品はプエルトリコの小売店で販売されていた4ロットが対象となり、ラベル上で「コロナウイルスとインフルエンザの感染対策に役立つ」と明記していたことが問題視されました。
FDAは即座に注意喚起情報を公表し、流通業者からの指摘により発覚したこの違反表示について、企業に対して製品製造の一時停止を要請しました。60カプセル入りボトル全量が市場から回収され、購入者には全額返金が行われています。この時点で健康被害の報告はありませんでしたが、企業は表示是正まで当該製品の製造販売を中止する措置を取りました。
Natural Solutions Foundation社の強制リコールケース
より深刻なケースとして、Natural Solutions Foundationが販売していた「Dr. Rima Recommends Nano Silver 10ppm」の事例があります。この銀含有サプリメントは、COVID-19の予防・治療・治癒効果を謳う表示を行っており、2020年1月から2021年12月までに販売された全ロットが対象となりました。
FDAはまず警告と販売差止めを要求し、その後司法当局を通じて法的措置に踏み切りました。2021年12月にFDAは同団体との間で恒久的差止命令に関する同意判決を締結し、2023年3月には過去販売分の完全回収を命じています。FDAの見解では、銀サプリメントを医療代替として使用することは適切な治療機会を逃し生命に危険を及ぼす可能性があるため、強制措置が正当化されました。
対象期間に販売された製品は徹底的に市場から撤去され、流通在庫や消費者手元の未使用品まで回収対象となりました。購入者と流通業者には返送要請と返金対応が行われ、同団体は今後このような違法表示製品を販売しないよう恒久的に命じられています。
疾病効果表示による製品差押えと廃棄処分の実例
FulLife社とCharron社の同時摘発
2007年には中小サプリメント企業による違法表示に対し、FDAが製品差押えという強制措置を実施しました。8月にはCharron Nutrition社のGlucobetic、Neuro-betic、Ocu-Compなど複数製品に対して約4.1万ドル相当が押収され、10月にはFulLife Natural Options社の「Charantea Ampalaya」約7.1万ドル相当が差し押さえられています。
これらの企業は糖尿病や関節炎などの深刻な疾患の治療効果を謳っており、FDAは度重なる警告にもかかわらず違反マーケティングを続けたため、司法省を通じて裁判所許可を得てU.S. Marshalsによる押収に踏み切りました。
違法表示の具体的内容と問題点
FulLife社の「Charantea Ampalaya」は血糖値を正常化すると称し、ウェブサイト上で「1型・2型糖尿病患者に強く推奨する」と宣伝していました。同社は「医薬品ではない」という免責文句を掲載していましたが、実質的に糖尿病治療を謳っており、FDAから見れば無承認医薬品の販売に該当します。
Charron社の製品群も同様に、糖尿病や関節炎その他の深刻な健康状態の治療に効くと宣伝されており、科学的証拠なしに疾病の予防・治療を標榜する誤表示を行っていました。
押収品の処分プロセス
押収された製品は司法当局に没収され、市場から強制的に排除されました。これら製品は違法医薬品扱いとなって流通が停止され、裁判所命令により廃棄処分または国外への廃棄的輸出となっています。米国法ではFDAによる輸入拒否品や押収品は原則として国内流通させず廃棄または再輸出処分とされるため、市場への再流入は完全に防がれました。
この強制措置により両社は当該商品の販売を続行できなくなり、違法表示による売上は没収される形となりました。行政処分の公表により企業イメージも損なわれ、他の業者への警告的効果も生まれています。
DSHEAに基づくサプリメント表示規制の法的枠組み
構造・機能表示と疾病効果表示の境界線
1994年に制定された栄養補助食品健康教育法(DSHEA)の下、サプリメントは医薬品ではなく食品カテゴリーとして扱われ、処方薬のような事前有効性審査を経ずに市場投入が可能です。FDAはサプリメントの発売前に効果や安全性を承認する権限を持たず、メーカー自身が製品の安全性や表示の適法性を担保する責任を負います。
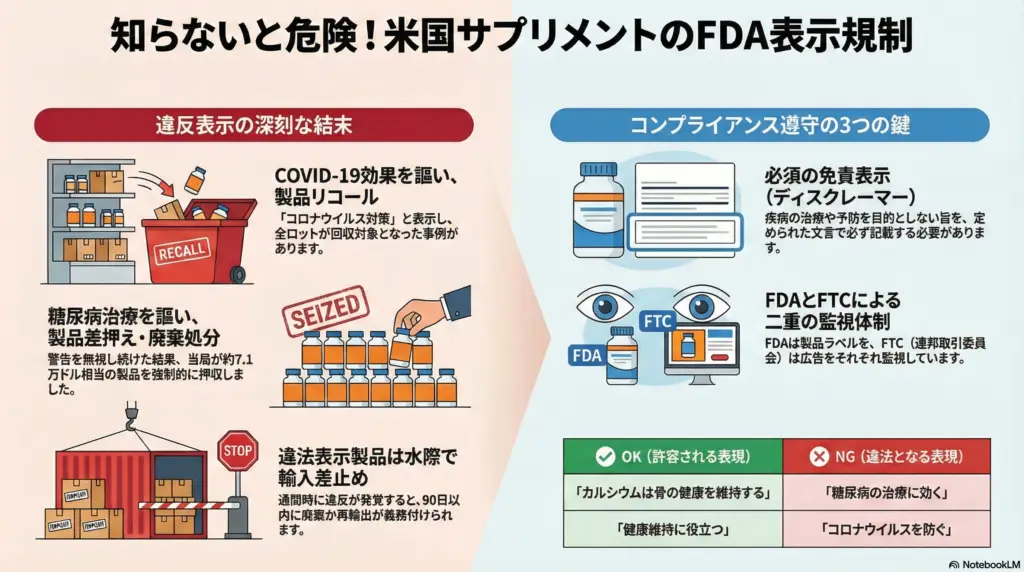
企業に許容されているのは疾病そのものの効果効能ではなく、構造・機能に関する主張です。例えば「カルシウムは骨の健康を維持するのに重要」といった、栄養素が人体の正常な構造や機能をサポートする表現は認められています。ビタミン欠乏症の予防に関する記述や健康維持に役立つといった一般的な健康増進の表現も一定範囲で許容されます。
必須となる免責ディスクレーマーの役割
これらの表示はFDAの事前承認を要さない自主的表示であるため、必ず免責文言の付記が法律で義務付けられています。典型的には「本製品に関する表示は米国食品医薬品局による評価を受けておりません。本製品は疾病の診断、治療、治癒、予防を目的としたものではありません」という文言であり、消費者に対してその効果がFDA認可ではないこと、疾病の診断・治療・予防を謳うものではないことを明示します。
この免責文言は医薬品だけが疾病効果を標榜できるという原則に基づいており、サプリメントが誤って医薬品的な効能を示唆しないための重要な規定となっています。
ヘルスクレームの承認プロセス
構造機能に関する表示とは別に、特定の疾病リスクの低減効果を直接謳うヘルスクレームはFDAが科学的証拠を精査した上で個別に許可した場合のみ表示できます。例えば「カルシウムの適切な摂取は骨粗鬆症リスクを低減する可能性がある」等の表現はFDA許可済みのヘルスクレームです。
企業が未承認の疾病予防・治療効果を謳うことは、たとえ間接的な表現であってもFDA規制に抵触するミスブランド違反となります。本記事で挙げた事例のように「○○を防ぐ」「○○患者に効果がある」などの表示は明確に禁止されており、健康詐欺製品と見なされ厳正な対処の対象となります。
FDAとFTCによる二重監視体制の実効性
広告規制におけるFTCの管轄権
サプリメントのラベル表示はFDAが所管しますが、テレビ・インターネット広告など商業広告における健康効果表示については連邦取引委員会が管轄します。FTC法の下では製品の広告において健康に関する主張を行う場合、信頼できる科学的根拠に裏付けられていなければならないとされています。
特に「特定の疾病を予防/治療できる」と謳う広告は医薬品レベルの厳格な証拠が無ければ虚偽広告と見做され、FTCは差止措置や罰金科措置を含む法執行を行います。過去10年間でFTCは120件以上のサプリメント関連健康クレームに対する法的措置を起こしています。
連邦・州レベルでの協調取締り強化
2019年にはFDA長官がアルツハイマー病などに効能を謳うサプリメントの蔓延に懸念を示し、FDAとFTCは共同で12社に対し「根拠のない疾病治療効果表示」をやめるよう警告書を発出しました。
2024年には記憶力向上サプリ「Prevagen」に対しFTCとニューヨーク州司法長官が共同提訴し、同製品の「脳機能・記憶力改善」効果を謳う広告を禁止する判決を勝ち取っています。連邦・州レベルで不実な健康表示への法的追及が強化されており、企業のコンプライアンスリスクは増大しています。
輸入差止めと水際での違法製品排除メカニズム
米国市場に流通するサプリメントには海外からの輸入品も多く含まれます。FDAは海外製サプリメントについても、ラベルが英語表示要件を満たさないものや疾病効果を謳うなどの違法表示が認められたものに対しては、輸入警告リストに掲載して通関段階で差し止める措置を取ります。
輸入差止めとなった製品は通関時に留保され是正の機会が与えられますが、是正できない場合には90日以内に輸出または廃棄することが義務付けられます。違反製品が勝手に国内に流通しないよう、FDA職員や税関の立会いの下で廃棄処分が行われる仕組みです。輸入業者が廃棄・再輸出に応じなければ罰則が科されるため、実質的に国外退去または廃棄以外の選択肢はありません。
このようにしてFDAは国内外からの違法表示サプリメントの流通を水際で防ぎ、国内市場の健全性を保つ努力をしています。
企業が直面する表示コンプライアンスリスクと対策
米国ではビタミンサプリメントに関する健康強調表示についてDSHEAによる緩和策と、FDA/FTCによる事後規制が組み合わさった体制が敷かれています。企業にとっては一定の表現の自由が認められる一方、消費者保護の観点から「疾病を治せる」等の誤解を招く表示は厳禁であり、違反すれば製品撤去や事業停止といった厳しい代償を招きます。
特にパンデミック以降、感染症予防を謳う製品への監視が強化されており、企業は表示文言の法的適合性を慎重に検討する必要があります。構造・機能表示と疾病効果表示の境界線を正確に理解し、必要な免責文言を適切に配置することが、リコールリスクを回避する最も確実な方法です。
米国市場に参入する企業や消費者は、サプリメントの表示ルールとそれを巡る規制当局の動向について正しく理解し、健全な商品選択・マーケティングを行うことが求められます。FDAの警告書発出から強制リコール、製品廃棄に至るまでの一連のプロセスを理解することで、企業は予防的なコンプライアンス体制を構築できるでしょう。
コメント